研究内容
私たちの研究室では、計算物理化学的アプローチと情報科学的アプローチを組み合わせることで生命現象を理解することを目標とし、研究を進めています。計算物理化学では分子動力学シミュレーションや量子化学計算を用い、情報科学では機械学習や構造インフォマティクスを活用することで生体分子の設計や制御方法を開発し、最終的には創薬へとつなげることを目指します。
研究テーマ
拘束条件付き拡散モデルによる生体分子複合体の構造予測と構造サンプリング
AlphaFold3に代表される拡散モデルベースの構造予測手法に対し、逆拡散過程に物理化学的な拘束条件を導入する独自の手法(restraint-guided inference)を開発しています。この枠組みにより、タンパク質-リガンド複合体の立体化学的精度の向上から、タンパク質の構造変化やリガンド解離経路のサンプリングまで、幅広い応用を実現しています。
-
タンパク質-リガンド複合体構造予測における立体化学的精度の改善:AlphaFold3やBoltz-1の予測構造に含まれるリガンドのキラリティ・結合長・結合角の誤りを、逆拡散過程への立体化学的拘束条件の導入により解決しました。 Improving Stereochemical Limitations in Protein-Ligand Complex Structure Prediction (ACS Omega, 2025)
-
距離拘束付き拡散モデルによるタンパク質構造変化とリガンド解離経路のサンプリング:Boltz-2の逆拡散過程に原子群間の重心距離拘束を導入し、再学習なしでタンパク質のopen-closed構造変化やペプチド解離経路を系統的にサンプリングする手法を開発しました。 Distance-Restraint-Guided Diffusion Models for Sampling Protein Conformational Changes and Ligand Dissociation Pathways (bioRxiv, 2026)
予測構造と計算化学シミュレーションによる生合成酵素・疾患関連酵素の機能解明
AlphaFold等による予測構造をMDシミュレーションやQM/MM計算と組み合わせることで、天然物生合成酵素や疾患関連酵素の反応機構を原子レベルで解明しています。生合成遺伝子クラスター(BGC)中のタンパク質複合体構造の予測にも取り組んでいます。
-
生合成遺伝子クラスター中のタンパク質複合体構造予測 Predicting protein complexes in biosynthetic gene clusters (bioRxiv, 2025)
-
ATP依存型ジアゾターゼCmaA6の触媒機構の構造基盤 Structural Basis for the Catalytic Mechanism of ATP-Dependent Diazotase CmaA6 (Angew. Chem. Int. Ed., 2025)
-
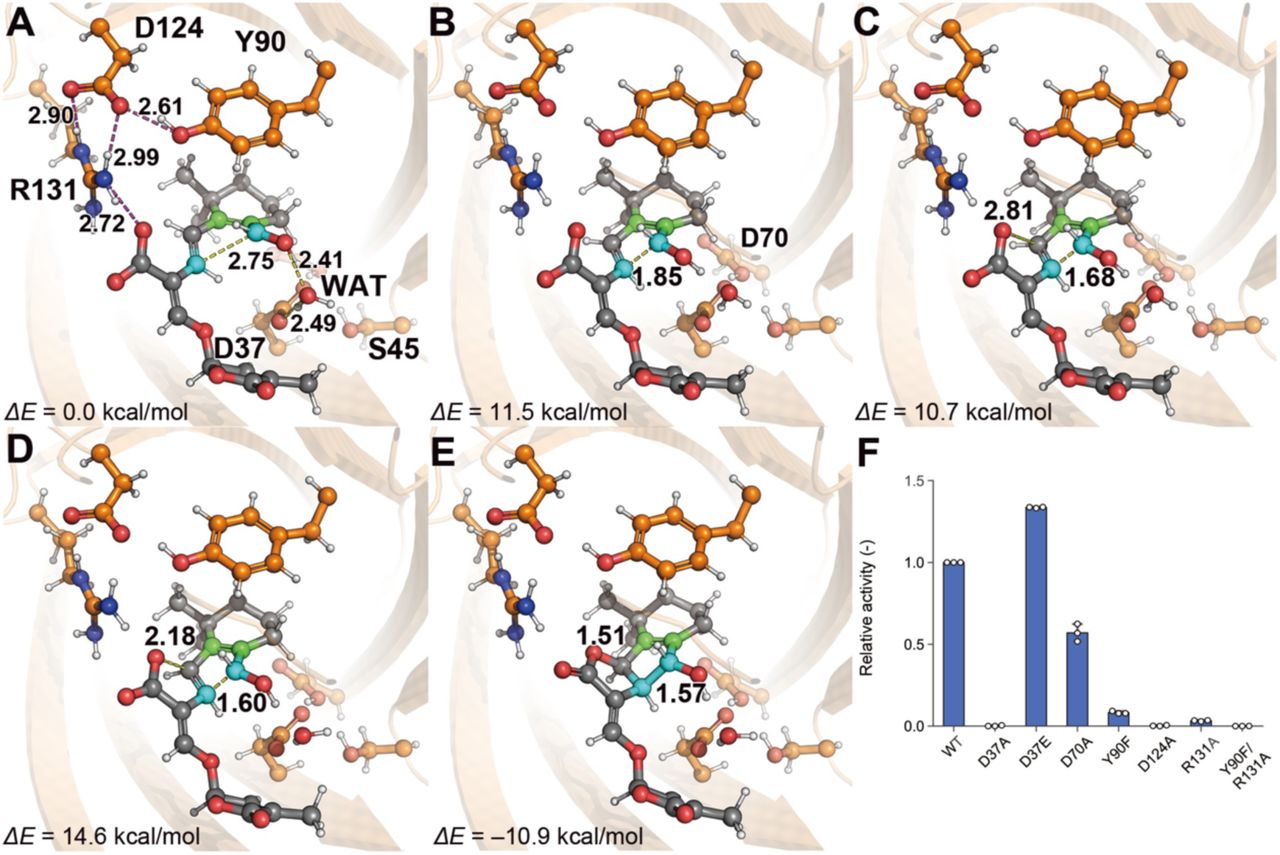
パーキンソン病関連タンパク質DJ-1による解糖系副産物分解の反応機構の解明 The reaction mechanism for glycolysis side product degradation by Parkinson’s disease-linked DJ-1 (J. Cell Biol., 2025)
-
リンコサミド生合成の多様化におけるPLP依存酵素の分子基盤 Molecular basis for the diversification of lincosamide biosynthesis by pyridoxal phosphate-dependent enzymes (Nature Chemistry, 2024)
-
AlphaFold2の予測構造とMDシミュレーション、QM/MM(ONIOM)法を組み合わせたストリゴラクトンの新規生合成機構の解明 Insights into stereoselective ring formation in canonical strigolactone: Discovery of a dirigent domain-containing enzyme catalyzing orobanchol synthesis (Proc. Natl. Acad. Sci. USA, 2024)
-
4″-メチル-SAMを基質とする4-メチルアゼチジンカルボン酸合成酵素 4″-Methyl-S-Adenosyl-l-Methionines Are Substrates for 4-Methylazetidinecarboxylic Acid Synthases (ACS Chemical Biology, 2026)
深層学習を用いた構造ベース創薬手法の開発
タンパク質の立体構造情報と化合物の化学的性質を深層学習で統合し、創薬プロセスの各段階(結合部位予測、化合物-タンパク質相互作用予測、分子設計)を加速する手法を開発しています。
-
構造・化合物言語モデルを統合した化合物-タンパク質相互作用予測(GenSPARC):タンパク質の3D構造を考慮したタンパク質表現と化合物の性質を考慮した言語モデル表現を組み合わせ、バーチャルスクリーニングへの汎化性能を実現しました。 Generalizable compound protein interaction prediction with a model incorporating protein structure aware and compound property aware language model representations (Communications Chemistry, 2026)
-
グラフトランスフォーマーによるリガンド結合部位予測:タンパク質の残基グラフに対しGraph Transformer を適用し、リガンド結合部位を高精度に予測する手法を開発しました。 Protein ligand binding site prediction using graph transformer neural network (PLoS ONE, 2024)
-
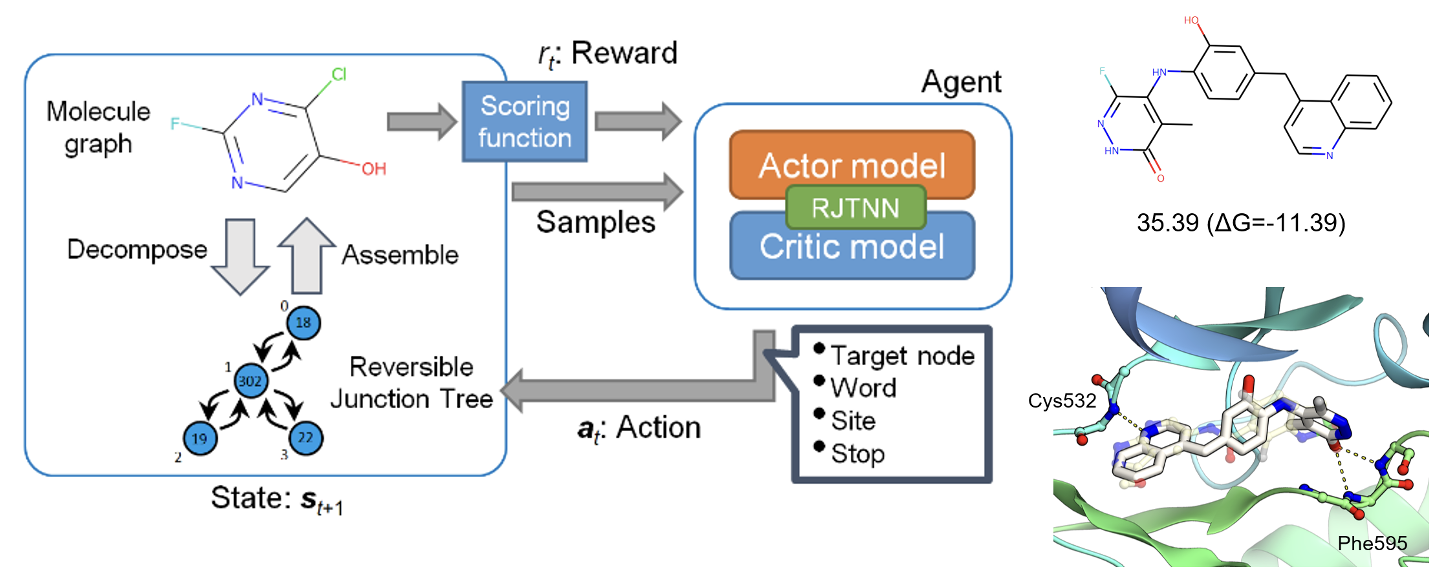
深層強化学習を用いた分子設計 Reinforcement learning-driven exploration of peptide space: accelerating generation of drug-like peptides
多目的最適化によるタンパク質設計
AI技術を活用したタンパク質設計において、構造類似性の維持と配列多様性の確保というトレードオフを多目的最適化により同時に解決する手法を開発しています。
- ProteinMPNNと多目的最適化アルゴリズムを組み合わせ、標的構造に類似しつつ配列の多様性を確保するタンパク質配列設計手法を開発しました。(CBI学会2025年大会 口頭発表賞受賞) Multi-objective optimization for designing structurally similar proteins with diverse sequences (Science and Technology of Advanced Materials: Methods, 2026)
AlphaFoldを用いたタンパク質複合体構造予測
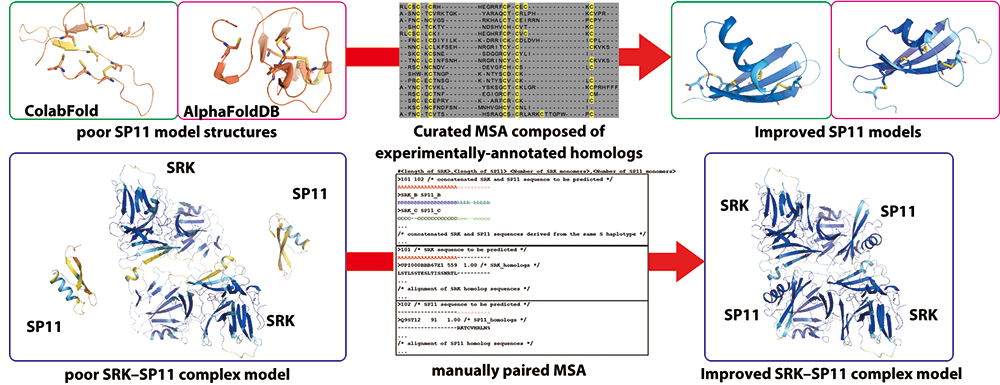
精選したMultiple Sequence Alignment(MSA)とColabFoldを用いることで、タンパク質複合体構造の高信頼度な予測を実現しています。ColabFoldの開発にも共著者として貢献しています。
-
アブラナ科の自家不和合性を制御するハプロタイプ特異的なSRK-SP11複合体の高信頼度予測 Comprehensive computational analysis of the SRK–SP11 molecular interaction underlying self-incompatibility in Brassicaceae using improved structure prediction for cysteine-rich proteins
-
ColabFoldプロトコル Easy and accurate protein structure prediction using ColabFold (Nature Protocols, 2024)
生体高分子の分子動力学シミュレーションによるダイナミクスの解明
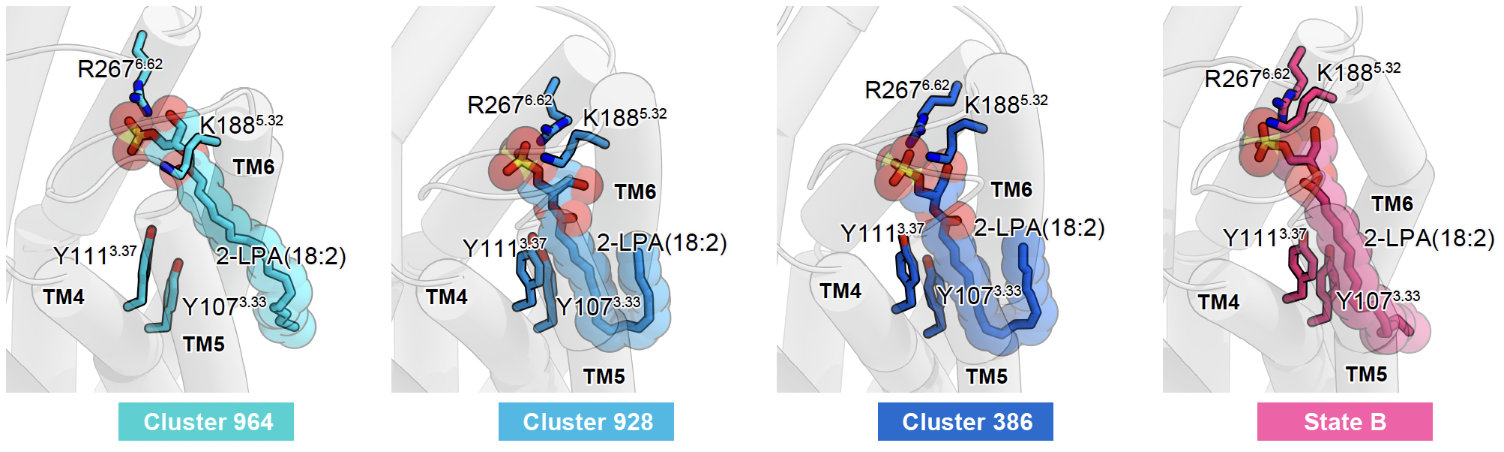
MDシミュレーションにより、GPCRなどの膜タンパク質のダイナミクスとシグナル伝達機構を解明しています。
- MDシミュレーションによるGPCRのダイナミクスとシグナル伝達機構の解明
LPA6受容体の側方アクセス機構の検証